단국대학교 RNA 세포생물학 국가지정 연구실
2011-04-05
정선주(sjsj)
- 8347
- 0


RNA Biology: RNA World and Beyond
최근 생물학 연구분야 중에서 가장 괄목할 만한 성장을 한 분야는 “RNA 생물학(RNA Biology)”이다. 1953년 Watson과 Crick의 DNA 구조 발견과 더불어 시작한 20세기 분자생물학에서, RNA는 DNA 유전정보를 단백질로 만드는 유전자발현의 중간과정에 생성되는 미미한 존재 정도로 평가되었다. 그러나 1980년대의 기념비적인 연구결과, RNA는 DNA와 단백질 사이의 단순한 전달자가 아니라 자체적으로 기능을 하는 RNA 효소(Ribozyme)일 수 있고 단백질에 비견될 만큼 다양하고 복잡한 작용을 하는 분자라고 제안되었다. 이에 따라 원시세포는 DNA나 단백질이 없이도 RNA 가 유전자이며 기능자인 "RNA 세계(RNA World)" 였을 것이라는 가설이 제기되었다. 다시 말하자면, RNA는 생명현상의 조연인 단순한 전달자에서 주연인 복합 기능자로 거듭나게 되었다. 이렇듯 가파른 RNA의 위치 상승에 기여한 공로로 Cech와 Altman은 1989년 노벨 화학상을 수상하였다.
1990년대에는 RNA의 예측하지 못한 중요한 기능이 또 발견되었다. 아주 작은 크기의 RNA가 여러 종의 세포에 존재하고 이들이 유전자의 발현을 조절한다는 것이 발표되면서, 이 RNA 간섭현상(RNA interference)의 중요성이 부각되었다. 작은 간섭 RNA(small interfering RNA, siRNA)가 주요 조절자로 작용하는 이 현상은 동물세포에서 특히 유용한 기술로서 많이 이용되고 있다. 동물세포에서는 특정유전자를 제거하는 것이 어렵기 때문에 siRNA를 이용한 유전자발현 억제방법(knock-down)은 특별히 귀한 기술이 되었다. 무엇보다 중요한 발전은 이렇게 작은 RNA가 신개념의 RNA 표적 신약개발의 초석이 된 것이다. 그래서 다시 한 번 RNA의 중요성이 크게 부각되면서, 2006년에 siRNA를 발견하고 연구한 공로로 Fire와 Mello가 RNA 분야에서 두 번째로 노벨상을 수상하였다.
단백질을 만들지도 않으면서 유전체(genome)에 존재하는 DNA를 junk DNA라고 부르기도 하였다. 그런데 이렇게쓰레기라고 생각한 DNA 중에 숨어서 RNA만 만들고 단백질을 만들지 않는 비암호화 RNA(non-coding RNA, ncRNA)가 있다. 이 들 중에는 miRNA처럼 크기가 작은 경우도 있지만 길이가 긴 것도 최근에 많이 발견되기 시작하였다. 어떤 종류의 ncRNA가 있는지, 이 들이 어떤 기능을 하는지, 왜 만들어 지는지 등은 이제서야 막 연구되기 시작한 미래의 보고라고 할 수 있다. 본 연구실은 이와 같이 새로운 패러다임으로 부상한 RNA의 세포내 신규 기능을 밝히고자 하는 목표를 가지고 있으며 2008년에 RNA Cell Biology Lab으로 국가지정연구실(NRL)에 선정되어 연구에 정진하고 있다.
RNA Binding Proteins: Expanding the Scope of RNA
위와 같이 RNA는 그 다양성과 기능성의 측면에서 기존의 단순전달자라는 설을 뛰어 넘을 정도로 종류가 많고 그 기능 또한 놀라울 정도로 다양하고 획기적이다. 그렇다면 RNA는 이런 중요한 기능을 단독으로 수행할 수 있을까? 그렇지는 않다. 세포 안에서 RNA는 항상 RNA 결합단백질(RNA Binding Protein, RBP)과 결합하여 RNA 복합체(RiboNucleoProtein complex, RNP)를 형성한다. RNP 복합체는 RNA 생성단계나 세포내 작용위치, 작동방법 등 여러 요인에 따라 복합적이고 다이나믹하게 형성되고 작동한다 (그림 1). 이와 같은 RNA와 RBP 들의 상호작용에 의한 RNP는 세포를 정상적으로 작용하게 하는 중요한 RNA 네트워크이다. 그러므로 본 연구실의 주요 연구목표는 다양한 RNA 대사과정(RNA Metabolism)을 조절하는 RBP를 발굴하고 이 들의 새로운 기능을 밝히는 것이다. 이를 위하여 신규 RBP 발굴과 확인을 위한 다수의 RNA-단백질 상호작용 분석 방법, RNA 대사과정을 분석하는 다양한 Cell based assay가 필요하다. 본 연구실원들은 전통적인 생화학, 분자생물학, 세포생물학적 RNA 관련 기술을 구축하였고 global RNA-RBP 네트워크 분석을 위한 최신의 실험 방법들을 정립하기 위해 노력하고 있다.

Altered RNA Network: Finding Novel Therapeutic Targets
이렇게 중요하고 다양한 RNA가 잘못 만들어 지면 어떻게 될까? 그 한가지 예를 선택적 RNA 스플라이싱(Alternative RNA Splicing, AS-RNA)에서 찾을 수 있다. AS-RNA는 적은 수의 유전자에서 상황에 따라 입맛에 맞게 RNA를 제작하여 세포의 기호에 맞는 단백질을 만드는 방법이다. 만약 어떤 세포에서 이상한 AS-RNA가 만들어 지면 단백질까지도 잘못 만들어 질 수 있고 세포의 기능도 비정상으로 될 것이다. 이상하게 발현되는 RNA가 여러 종류의 암이나 신경계 및 근육계 질환에서 자주 발견되는 것으로 보아 이러한 질환의 원인은 비정상적인 RNA 네트워크 조절일 가능성이 높다 (그림 2).
최근 연구결과 특히 암세포에서 잘못 발현되는 RNA나 RBP들이 속속 밝혀지고 있다. 앞으로 해야 할 중요한 연구는 정상세포에서와 달리 암세포에서만 발현되는 AS-RNA나 ncRNA를 암세포의 마커로 발굴하고, 이를 비정상적으로 조절한 RBP를 찾아 내어 그 기능을 차단하고 조절하는 것일 것이다. 다시 말하자면, 질환관련 비정상 RNA 네트워트를 발굴하고 제어하는 것이 중요한 연구방향이다. 그러므로 본 연구실에서는 RNA metabolism의 필수 조절인자로서 발굴한 새로운 RBP가 암세포에서 비정상적으로 과발현되거나 자신의 기능을 제대로 하지 못하는 기전을 연구하여 항암제 신약개발의 표적을 제공하고자 한다.

RNA Aptamer: Utilizing the Power of RNA
RNA World 가설을 확실히 증명하는 방법은 단백질처럼 작용하는 RNA를 발견하는 것이다. 그러나 현생세포에 자연적으로 존재하는 RNA는 기능적인 측면을 단백질에 이양하며 진화하였기 때문에 원시세포에서처럼 단백질과 같이 작용할 RNA는 많지 않을 것이다. 그렇다면 “시험관에서 진화 (in vitro evolution)”를 시켜보면 원시 RNA와 같은 기능체 RNA를 발견할 수 있지 않을까 하는 의견이 대두되기 시작하였다. 다양성이 매우 높은 (>1015 이상의 다양한 서열을 가진 RNA가 섞여 있는) RNA 라이브러리로부터 가장 적합한 RNA 분자를 찾는 기술을 적용하면 기능체 RNA를 얻을 수 있었다. 일반적으로 RNA 라이브러리는 40개 이상의 random sequence와 양 끝의 defined sequence를 갖는 RNA 분자들이 혼합된 상태이다. 1990년 Colorado 대학의 Larry Gold는 이러한 방법에 SELEX (Systemic Evolution of Ligands by EXponential Enrichment)라는 이름을 명명하였다. 같은 해에 같은 방법으로 여러 다양한 분자에 결합하는 RNA 분자들이 발견되기 시작하면서 RNA는 저분자 화합물부터 고분자 단백질에 이르기 까지 여러 종류의 표적 분자에도 결합할 수 있는 있음이 여러 연구실에서 보고되었다. 즉, SELEX 방법은 RNA World 가설을 지지하는 근거를 제시하는 중요한 단서가 되었다.
이렇게 발굴된 RNA 분자는 라틴어의 Aptus (fitting)라는 단어를 따서 Aptamer라 불리게 되었고 이후 오랜 기간동안 전 세계 우수한 연구진들의 손을 거쳐 좀 더 진화된 형태로 개발되어 왔다. 암에 대한 RNA aptamer는 연구에 있어서도 아직 초기 단계이다. VEGF를 표적으로 하는 Macugen의 경우에도 angiogenesis 억제를 할 수 있으므로 항암제로서 개발하기 위한 시도를 하고 있다. 암세포의 경우에는 정상세포와는 달리 신호전달체계가 작동하므로, 이를 표적으로 한 RNA aptamer가 선별되어 치료제로서의 개발 가능성이 타진되고 있다.
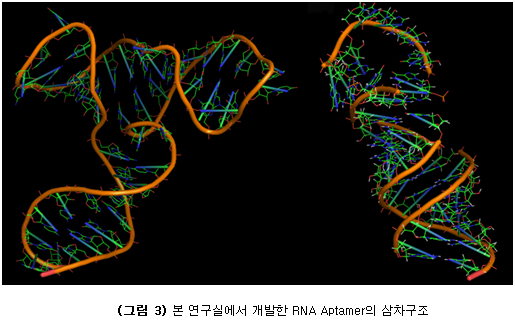
본 연구실에서 개발한 RNA aptamer는 대장암세포에서 과다하게 작동하는 Wnt/β-catenin 신호전달계를 표적으로 하여 개발되었다 (그림 3). 본 연구에서는 RNA aptamer를 DNA 형태로 세포내에 주입 후 발현시키는 RNA intramer로 개발하였고 표적 단백질인 β-catenin의 세포 내 기능을 억제함을 보였다. 이에 따라 대장암에서 과다 작용하는 β-catenin의 기능을 조절하는 치료법으로 개발될 수 있음을 제안하였다. 이러한 기초 연구는 아직 초기이기는 하지만 암에 대한 유전자 치료제로서 RNA aptamer가 활용될 수 있다는 가능성을 보여준다. 또한 최근에는 유방암의 치료 및 진단을 위하여 ErbB2 단백질을 표적으로 하는 RNA aptamer를 개발하여, in vivo imaging에 활용할 수 있는 가능성을 연구하고 있다 (그림 3).
RNA World 가설을 확실히 증명하는 방법은 단백질처럼 작용하는 RNA를 발견하는 것이다. 그러나 현생세포에 자연적으로 존재하는 RNA는 기능적인 측면을 단백질에 이양하며 진화하였기 때문에 원시세포에서처럼 단백질과 같이 작용할 RNA는 많지 않을 것이다. 그렇다면 “시험관에서 진화 (in vitro evolution)”를 시켜보면 원시 RNA와 같은 기능체 RNA를 발견할 수 있지 않을까 하는 의견이 대두되기 시작하였다. 다양성이 매우 높은 (>1015 이상의 다양한 서열을 가진 RNA가 섞여 있는) RNA 라이브러리로부터 가장 적합한 RNA 분자를 찾는 기술을 적용하면 기능체 RNA를 얻을 수 있었다. 일반적으로 RNA 라이브러리는 40개 이상의 random sequence와 양 끝의 defined sequence를 갖는 RNA 분자들이 혼합된 상태이다. 1990년 Colorado 대학의 Larry Gold는 이러한 방법에 SELEX (Systemic Evolution of Ligands by EXponential Enrichment)라는 이름을 명명하였다. 같은 해에 같은 방법으로 여러 다양한 분자에 결합하는 RNA 분자들이 발견되기 시작하면서 RNA는 저분자 화합물부터 고분자 단백질에 이르기 까지 여러 종류의 표적 분자에도 결합할 수 있는 있음이 여러 연구실에서 보고되었다. 즉, SELEX 방법은 RNA World 가설을 지지하는 근거를 제시하는 중요한 단서가 되었다.
이렇게 발굴된 RNA 분자는 라틴어의 Aptus (fitting)라는 단어를 따서 Aptamer라 불리게 되었고 이후 오랜 기간동안 전 세계 우수한 연구진들의 손을 거쳐 좀 더 진화된 형태로 개발되어 왔다. 암에 대한 RNA aptamer는 연구에 있어서도 아직 초기 단계이다. VEGF를 표적으로 하는 Macugen의 경우에도 angiogenesis 억제를 할 수 있으므로 항암제로서 개발하기 위한 시도를 하고 있다. 암세포의 경우에는 정상세포와는 달리 신호전달체계가 작동하므로, 이를 표적으로 한 RNA aptamer가 선별되어 치료제로서의 개발 가능성이 타진되고 있다.
본 연구실에서 개발한 RNA aptamer는 대장암세포에서 과다하게 작동하는 Wnt/β-catenin 신호전달계를 표적으로 하여 개발되었다 (그림 3). 본 연구에서는 RNA aptamer를 DNA 형태로 세포내에 주입 후 발현시키는 RNA intramer로 개발하였고 표적 단백질인 β-catenin의 세포 내 기능을 억제함을 보였다. 이에 따라 대장암에서 과다 작용하는 β-catenin의 기능을 조절하는 치료법으로 개발될 수 있음을 제안하였다. 이러한 기초 연구는 아직 초기이기는 하지만 암에 대한 유전자 치료제로서 RNA aptamer가 활용될 수 있다는 가능성을 보여준다. 또한 최근에는 유방암의 치료 및 진단을 위하여 ErbB2 단백질을 표적으로 하는 RNA aptamer를 개발하여, in vivo imaging에 활용할 수 있는 가능성을 연구하고 있다 (그림 3).
β-Catenin: Discovering as a Novel RBP for RNA Network in Cancer Cells
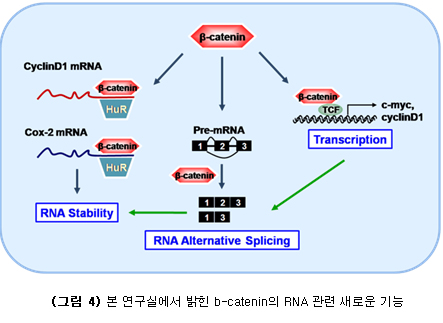
β-Catenin은 대장암과 유방암을 비롯한 여러 암세포에서 비정상적으로 과발현되거나 돌연변이가 일어나 여러 표적 유전자의 발현을 조절하여 암세포의 분화, 발생 및 전이 과정에 영향을 미치는 단백질이다. β-Catenin의 주요 기능은 핵에서의 전사조절인자임이 잘 알려져 있는데, 본 연구실에서는 핵내에서의 β-catenin이 다수의 유전자의 발현을 조절하는 과정에서 chromosome looping을 조절함을 새롭게 밝혀내었다. 특히 흥미로운 발견은 β-catenin 단백질의 중앙에 있는 armadillo 반복서열에 RNA가 결합할 수 있다는 것이고 이 domain에 특이적으로 결합하는 RNA aptamer를 개발하여 연구에 신뢰도를 높였다. 또한 β-catenin이 세포질에 있을 때 세포접합부위에 있거나 단백질이 분해됨이 정설로 보고되었지만, 그 외에도 Cyclooxygenase-2나 CyclinD1과 같이 암을 유발시키는 mRNA의 3’-UTR에 결합하여 RNA stability를 조절하여 β-catenin이 RNA 네트워크의 조절 인자로서 작용함을 제시하였다. 현재 본 연구실에서는 여러 명의 대학원생들이 β-catenin의 새로운 기능을 찾기 위해 열심히 연구에 매진하고 있으며 아직 밝혀지지 않은 β-catenin에 의한 Cellular transcriptome의 post-tranacriptional level에서의 작용 기전 탐색이 현재 본 연구실의 가장 큰 연구목표이기도 하다.
β-Catenin은 대장암과 유방암을 비롯한 여러 암세포에서 비정상적으로 과발현되거나 돌연변이가 일어나 여러 표적 유전자의 발현을 조절하여 암세포의 분화, 발생 및 전이 과정에 영향을 미치는 단백질이다. β-Catenin의 주요 기능은 핵에서의 전사조절인자임이 잘 알려져 있는데, 본 연구실에서는 핵내에서의 β-catenin이 다수의 유전자의 발현을 조절하는 과정에서 chromosome looping을 조절함을 새롭게 밝혀내었다. 특히 흥미로운 발견은 β-catenin 단백질의 중앙에 있는 armadillo 반복서열에 RNA가 결합할 수 있다는 것이고 이 domain에 특이적으로 결합하는 RNA aptamer를 개발하여 연구에 신뢰도를 높였다. 또한 β-catenin이 세포질에 있을 때 세포접합부위에 있거나 단백질이 분해됨이 정설로 보고되었지만, 그 외에도 Cyclooxygenase-2나 CyclinD1과 같이 암을 유발시키는 mRNA의 3’-UTR에 결합하여 RNA stability를 조절하여 β-catenin이 RNA 네트워크의 조절 인자로서 작용함을 제시하였다. 현재 본 연구실에서는 여러 명의 대학원생들이 β-catenin의 새로운 기능을 찾기 위해 열심히 연구에 매진하고 있으며 아직 밝혀지지 않은 β-catenin에 의한 Cellular transcriptome의 post-tranacriptional level에서의 작용 기전 탐색이 현재 본 연구실의 가장 큰 연구목표이기도 하다.


2008-현재 RNA 세포생물학 국가지정연구실 책임교수
2006-현재 BK21 RNA 전문연구인력 양성사업팀 사업팀장
1995-현재 단국대학교 분자생물학과 및 나노센서바이오텍연구소 교수
2006-2008 단국대학교 국제교류처 처장
2005-2006 미국 UC San Diego 방문 연구원
1994-1995 서울대학교 유전공학연구소 연수 연구원
1990-1993 미국 Stanford 대학교 박사후 연구원
1986-1990 미국 Utah 대학교 이학박사
1981-1985 서울대학교 생명과학부 이학사

1993년에 단국대학교 한남동캠퍼스에 분자생물학과가 개설된 후 1995년 최초의 전임교수로 부임한 정선주교수가 1명의 석사과정생과 1명의 학부생과 함께 1997년에 처음 연구실을 열었다. 현재는 박사과정 6명, 석사과정 3명, 학부생 3명, 석사후 연구원 2명, BK21 연구교수 1명, 재정을 책임지고 관리해 주는 친절한 조교까지 16명으로 연구실 가족이 늘었다. 2008년에 NRL에 선정되기 전 까지는 5~8명의 학부생과 석사과정 학생이 속해있는 아담한 규모로 운영되어 왔다. 점차 다양한 연구성과와 과제수행을 통하여 대내외적으로 이름이 알려졌고 그에 따라 연구실로 점점 많은 학생들이 모여 지금은 이렇게 큰 규모의 실험실이 되었다. 2007년에 단국대학교가 한남동캠퍼스를 경기도 용인시 수지구 죽전동으로 이전한 후, 학교측에서 연구실 학생들이 좀 더 편하게 연구 할 수 있도록 물심양면 배려해 주신 덕택에 현재 2개 실험실의 넓은 공간에서 불편함 없이 마음껏 연구활동을 수행하고 있다. 서울 교외의 여유로움과 분당권의 편리함, 죽전 법화산의 맑은 공기 속에서 연구에 전념할 수 있는 환경이 조성된 것이다.
아래 그림은 우리 멤버들의 소개를 cell signaling pathway로 나타내어 본 그림이다 (그림 5). 연구실 멤버 전체가세포내 정교한 신호전달처럼, 교수님의 에너지와 지식이 우리 연구원들에게 전달되고 그에 따라 일사불란하게 움직이는 모습을 표현해 보았다.
아래 그림은 우리 멤버들의 소개를 cell signaling pathway로 나타내어 본 그림이다 (그림 5). 연구실 멤버 전체가세포내 정교한 신호전달처럼, 교수님의 에너지와 지식이 우리 연구원들에게 전달되고 그에 따라 일사불란하게 움직이는 모습을 표현해 보았다.

놀 때는 놀고 공부할 때는 공부하자는 연구실의 모토는 집중과 휴식의 중요성을 잘 보여준다. 몸과 마음이 지칠 때쯤 되면 재충전을 위한 MT를 통해 실험실을 벗어나 대자연의 품에 안겨 호연지기를 배우고 멤버들 간의 단합도 도모하는데, 이런 휴식의 시간은 1년에 두 번 정도이다 (그림 6).

MT도 즐겁지만 더불어 학문적 소양과 식견을 넓힐 수 있는 학회 참가는 더없이 귀한 기회가 된다. 특히 같은 분야를 공부하는 학생들과 연구내용도 공유하고 대화의 장을 가지며 학생들은 미래의 꿈을 키워간다 (그림 7). 아직 대학교 공부를 마치지 않은 학부생들도 학회에 참석하여 포스터 발표의 기회를 갖기도 하는데 이런 특별한 경험들은 연구에 대한 동기를 부여해 주고 미래에 대한 비전을 갖게 해 준다. 또한 학문적 시야를 세계적으로 넓힐 수 있는 외국학회 참석의 경우에는 교수님의 교육철학에 따라 학기의 높고 낮음에 상관없이 그 기회가 평등하게 주어진다. 외국학회에서 느끼는 지적 자극과 감흥은 아직 교과서적인 지식에 얽매여 굳어있는 학생들의 뇌를 더 유연하게 만들고, 더 나아가 우리의 연구활동 무대가 국내학계뿐 아니라 세계와도 연결되어 있음을 다시 한 번 느끼게 해 준다. 아직 어린 만큼 많은 지식을 얻어 오지는 못할지라도 “백문이 불여일견” 이라는 말처럼 몸소 체험하는 잊지 못할 경험들의 가치는 돈으로 값을 대신할 수 없는 것 같다.

BK21과 NRL 주관으로 주기적으로 개최하는 크고 작은 세미나에서는 국내뿐 아니라 RNA 생물학 분야에 널리 알려진 해외 유명 석학들을 초빙한다. 해외 연사들은 세미나실에서 최신의 연구업적을 발표할 뿐 아니라 본 연구실 학생들과 따로 만날 기회를 가져, 친밀한 대화와 질문을 통하여 현재의 지식을 넓힐 뿐 아니라 세계속의 과학자로 성장할 수 있는 바탕을 만들고자 한다 (그림 8).


이러한 분위기 속에서 남다른 유대감을 갖고 있는 우리 연구실 멤버들에게는 회식때 마다 등장하는 조금 특별한 건배 파이팅 구호가 있다.
‘우리는 팀이다^^ 서로 도와 세계 최고~ 정랩 파이팅!’
개개인의 능력을 합쳐서 더 큰 힘을 발휘하는 하나의 유기적인 팀이 되어, 앞에서 끌어주고 뒤에서 밀어주는 선후배간의 관계를 통해 세계최고가 되겠다는 구호가 실현되는 그 순간까지, 하루하루 한걸음 한걸음 최선을 다해 정진해 가는 정랩 멤버들! 늘 냉철한 과학자의 모습으로 연구를 지도하시고, 때로는 따뜻한 어머니 같이 보살펴 주시는 연구실의 영원한 방장 교수님! 모두모두 파이팅 입니다!
개개인의 능력을 합쳐서 더 큰 힘을 발휘하는 하나의 유기적인 팀이 되어, 앞에서 끌어주고 뒤에서 밀어주는 선후배간의 관계를 통해 세계최고가 되겠다는 구호가 실현되는 그 순간까지, 하루하루 한걸음 한걸음 최선을 다해 정진해 가는 정랩 멤버들! 늘 냉철한 과학자의 모습으로 연구를 지도하시고, 때로는 따뜻한 어머니 같이 보살펴 주시는 연구실의 영원한 방장 교수님! 모두모두 파이팅 입니다!

우리 연구실은 경기도 용인시 죽전동 126번지, 단국대학교 자연과학관 206호/317호에 위치해 있습니다.
우리 연구실의 문은 포근한 어머니와 같은 마음으로 언제나 열려 있습니다.
Tel : 031-8005-3163/3201
Fax: 031-8005-3164
Homepage : http://www.molcellbio.net
E-mail: sjsj@dankook.ac.kr


